LABORATORIO/GASES
INTRODUCCIÓN
Con este trabajo se busca explicar cada una de las leyes que rigen a los gases, mas específicamente las leyes de Boyle, la ley de Charles, la ley de avogadro y finalmente de la ley de los gases ideales y mostrando como se aplica cada una en los ejercicios














EJERCICIOS: ley de charles

















OBJETIVOS GENERALES
- Explicar las generalidades de las leyes existentes para los gases
- Dejar claras estas leyes y su aplicación
- Crear conocimientos claros de las leyes de los gases en las estudiantes
OBJETIVOS ESPECÍFICOS
- Explicar y dejar claro la aplicación y la teoría de la ley de Boyle
- Explicar y dejar claro la aplicación y la teoría de la ley de Charles
- Explicar y dejar claro la aplicación y la teoría de la ley de los gases ideales
- Explicar y dejar claro la aplicación y la teoría de la ley de avogadro
- Explicar detalladamente como se opera con estas leyes
MARCO TEÓRICO
LEY DE BOYLER
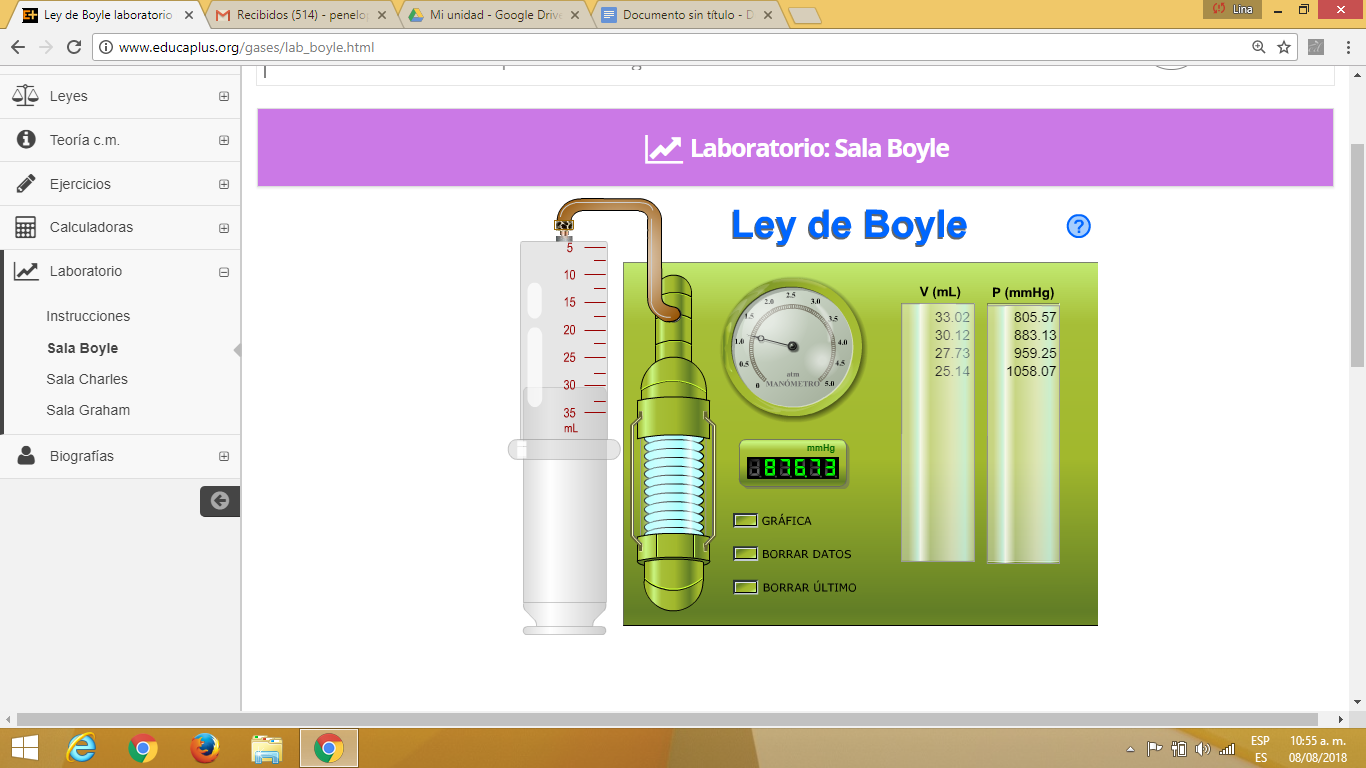
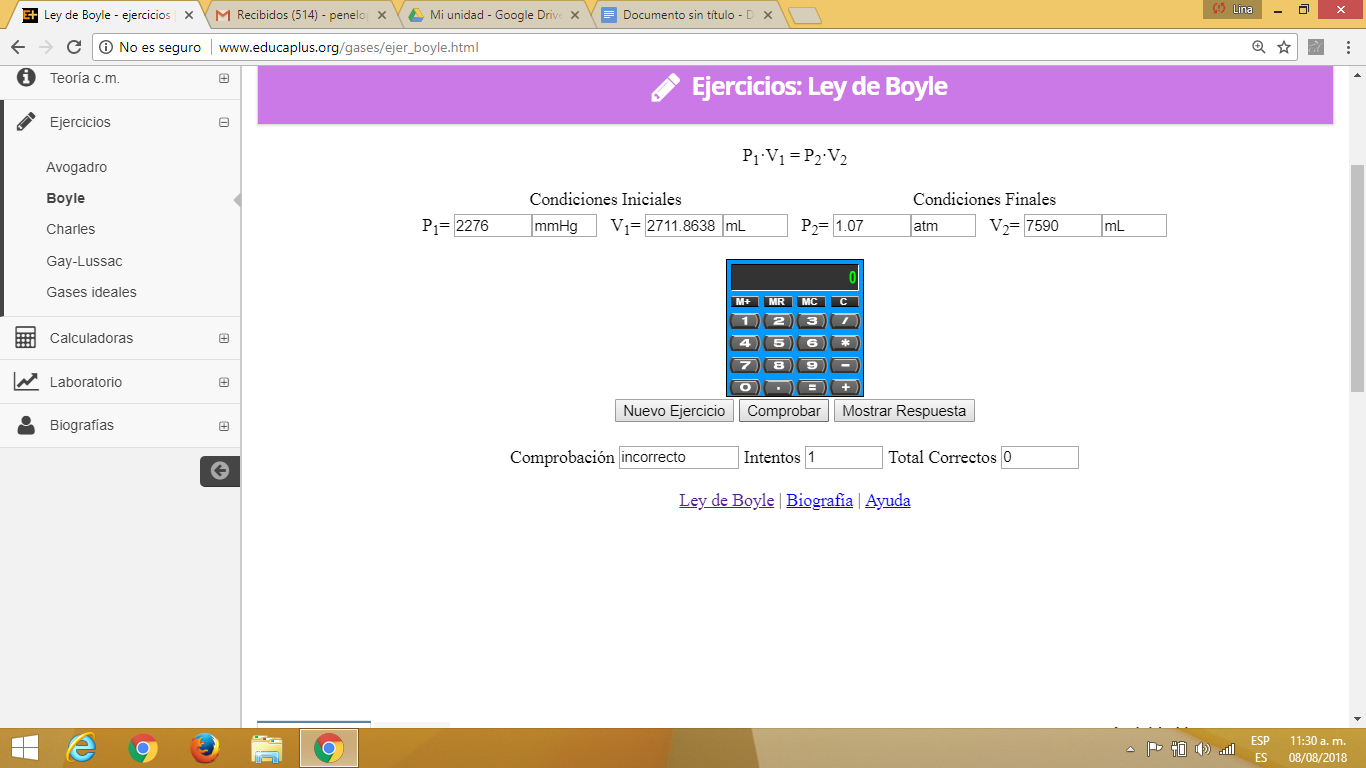
EJERCICIOS: ley de boyler
LEY DE CHARLES:
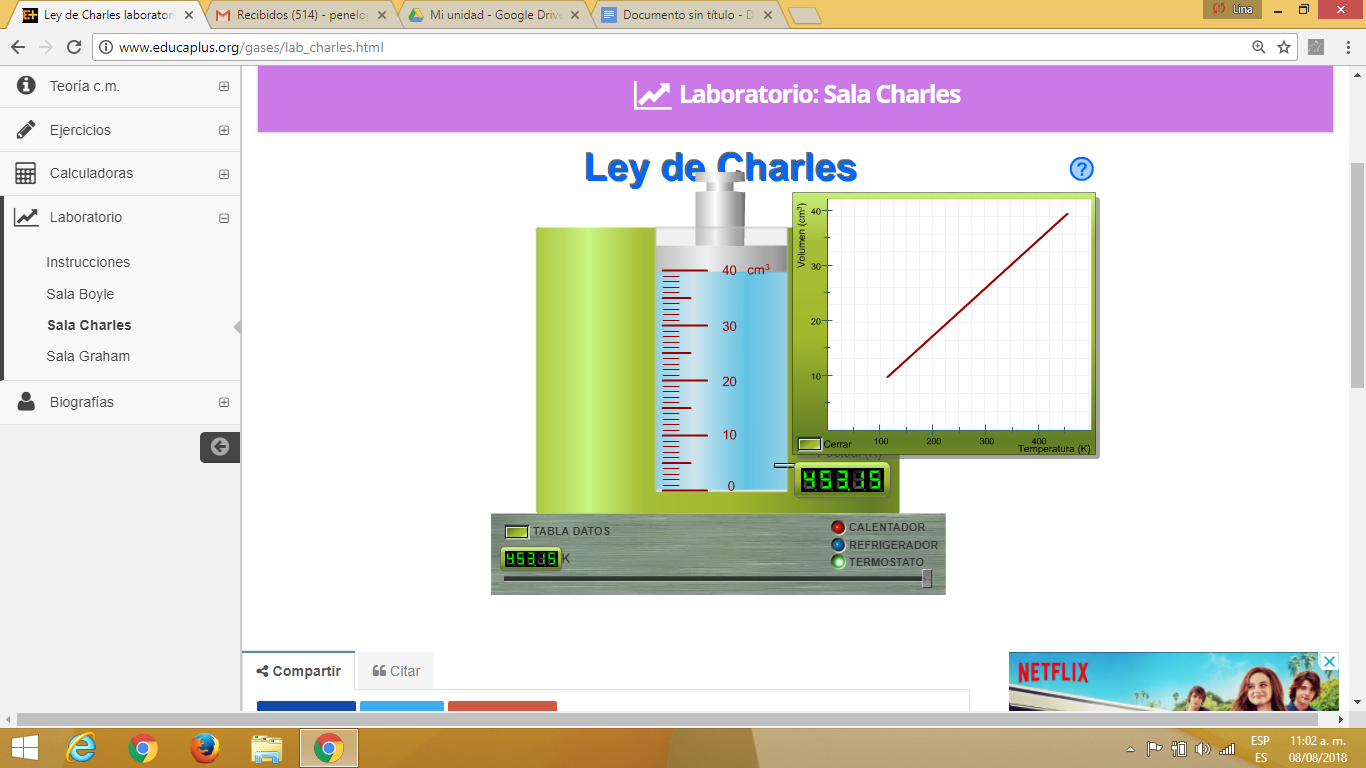
EJERCICIOS: ley de charles
LEY DE AVOGADRO
LEY DE LOS GASES IDEALES


CONCLUSIONES
- La ley de Charles nos dice que estudió por primera vez la relación entre el volumen y la temperatura de una muestra de gas a presión constante y observó que cuando se aumentaba la temperatura el volumen del gas también aumentaba y que al enfriar el volumen disminuía.
- La ley de Boyle Mariott establece que la presión de un gas en un recipiente cerrado es inversamente proporcional al volumen del recipiente, cuando la temperatura es constante.
- La ecuacion de los gases ideales concluye que la presion multiplicada por el volumen es igual al numero de moles multiplicado por la constante de proporcionalidad y por la temperatura











Comentarios
Publicar un comentario